隨著時間的推移,新冠疫苗利好消息接踵而來。
2月25日,國家藥監局附條件批準兩家公司新冠疫苗注冊申請。
一款是讓國人等待多時的康希諾的重組新型冠狀病毒疫苗(5型腺病毒載體)(商品名為「克威莎™」),這是首家獲批的國產腺病毒載體新冠病毒疫苗;一款是國藥中生武漢公司新型冠狀病毒滅活疫苗(Vero細胞)。
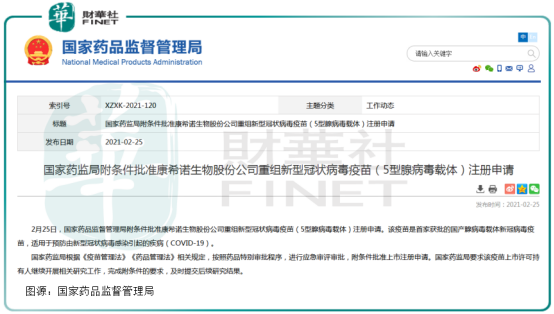
國產腺病毒載體新冠病毒疫苗姗姗來遲。
第一時間,A股、hth登录入口网页上市公司康希諾也分享了這一好消息。
重組新型冠狀病毒疫苗(5型腺病毒載體)是康希諾與軍事科學院軍事醫學研究院陳薇院士團隊共同開發研製,也是唯一採用單針免疫程序的新冠疫苗。
其採用基因工程方法構建,以複製缺陷型人5型腺病毒為載體,可表達新型冠狀病毒S抗原,以用於預防新型冠狀病毒感染引起的疾病。
目前疫苗已經在巴基斯坦、墨西哥、俄羅斯、智利、阿根廷5個國家開展全球多中心Ⅲ期臨床研究,已完成4萬餘受試者的接種及期中數據分析。
據公司公告,其Ⅲ期臨床試驗期中分析數據結果顯示:在單針接種疫苗28天後,疫苗對所有症狀的總體保護效力為65.28%;在單針接種疫苗14天後,疫苗對所有症狀總體保護效力為68.83%。疫苗對重症的保護效力分别為:單針接種疫苗28天後為90.07%;單針接種疫苗14天後為95.47%。
和重組新型冠狀病毒疫苗(5 型腺病毒載體)一起獲批的還有國藥集團中國生物武漢生物製品研究所有限責任公司的一款滅活疫苗(Vero細胞)。
國藥集團是「國家隊」,在2020年12月30日其中國生物北京生物製品研究所有限責任公司的新型冠狀病毒滅活疫苗(Vero細胞)已經或注冊申請,成為首家獲批的國產新冠病毒滅活疫苗。
至此中國已有4款新冠疫苗獲批上市,其中包括3款新冠滅活疫苗(國藥集團2款,北京科興1款)和1款腺病毒載體疫苗。
在中國市場,除了上述4款自主研發的新冠疫苗外,復星醫藥獲BioNTech SE授權在中國大陸及港澳台獨家代理mRNA 新冠疫苗。
2021年1月25日,mRNA新冠疫苗BNT162b2已經在中國香港獲緊急使用認可,但在中國内地尚未上市。
在全球抗擊新冠疫情的緊張時刻,中國上述自主研發的疫苗已經獲多國獲批緊急使用權,在抗疫中發揮了重要的作用。
自從2020年底新冠疫苗投入使用,新冠疫苗確實在全球抗疫中發揮了巨大作用。
據中泰證券研報顯示,截止2月22日全球累計接種2.12億劑次,2.8%左右人口至少接種過1劑次。
其中,美國(6418萬劑)、中國(4052萬劑)、歐盟(2753萬劑)、英國(1835萬劑)、印度(1142萬劑)、以色列(754 萬劑)等總接種量位居前列。
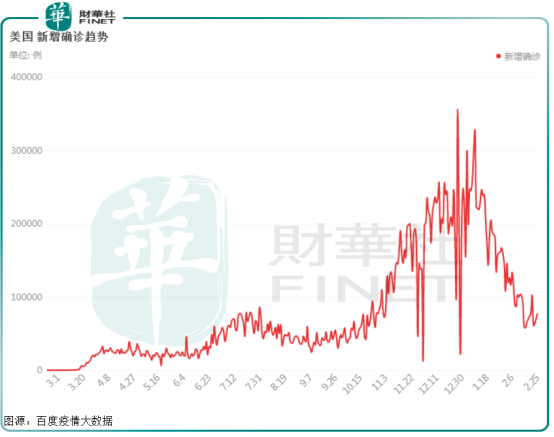
而隨著疫苗接種,美國新冠發病率在1月中旬達到歷史最高水平後,一直呈下降趨勢,每日新感染病例和死亡人數的平均值也在連續下降。
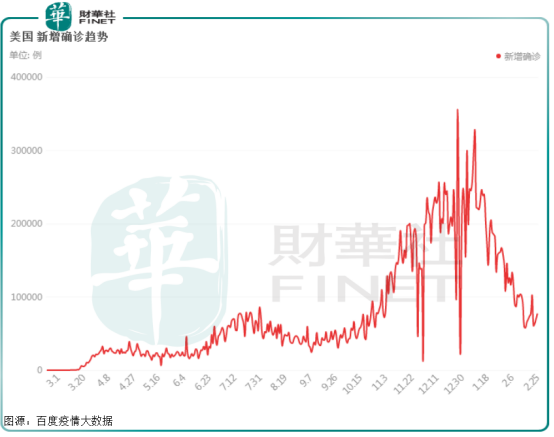
在上市服役的新冠疫苗中,全球主要有8款新冠病毒疫苗獲批上市,臨床試驗保護率均達到WHO要求的50%以上。
其中包括,BioNTech和輝瑞的BNT162b2(保護率95%)、Moderna的mRNA-1273(保護率94.1%)、阿斯利康/牛津大學的腺病毒載體疫苗AZD1222(保護率66.7%)、國藥集團的2款滅活疫苗(保護率79.34%)、科興生物的滅活疫苗(保護率50%以上)、俄羅斯Gamaleya 研究所的腺病毒疫苗Sputnik V(保護率91.6%)以及康希諾的重組新型冠狀病毒疫苗(5型腺病毒載體)已獲批上市。
此外,據中泰證券最新研究,Novavax、強生臨床Ⅲ期進展順利、已取得積極數據,智飛生物、康泰生物、復星醫藥等關鍵臨床(Ⅲ期/Ⅱ期橋接試驗)也順利推進中。
和康希諾同為病毒載體疫苗技術路線的是強盛和阿斯利康,均為單針接種,阿斯利康已經上市,強生已進入申報上市階段。
目前康希諾生物腺病毒載體新冠疫苗已經在墨西哥和巴基斯坦獲得緊急使用授權,還獲得墨西哥衛生部的3500萬劑新冠疫苗訂單。
最早獲批的國藥集團中國生物北京生物製品研究所滅活疫苗不僅免費供應國内,還援助埃及、白俄羅斯、阿根廷等國家。
根據杜克⼤學疫苗追蹤,截⾄2月15日,已有26個國家訂購了中國疫苗,分别是印度尼西亞巴西,智利,⼟耳其,摩洛哥,埃及,秘魯,菲律賓,巴基斯坦,馬來西亞,香港,烏克蘭,匈牙利,阿塞拜疆,阿拉伯聯合酋長國,哥倫比亞,泰國,烏拉圭,塞爾維亞,新加坡,墨西哥。
在目前已發揮作用的中國自主研發疫苗中,杜克大學數據顯示,科興疫苗最受歡迎,有12個國家訂購了科興疫苗。其中印度尼西亞訂購數量最多,共訂購1.4億劑疫苗(1.25億劑科興疫苗、0.15億劑康希諾疫苗)。
新冠疫苗陸續上市,讓早已在2020年就為之瘋狂的資本市場開始躁動,同時也有望複製核酸檢測出口盛況。
在康希諾新冠疫苗上市利好下,2月26日,康希諾A股和H股開盤大幅拉升,但最後雙雙卻以下跌收盤。
新冠疫苗主角股價短時難以衝高,與其業績有直接關係。2020年,康希諾營收實現同比增長990.06%,但歸母淨利潤卻為-40,704.64萬元,同比虧損增加159.63%。
新冠疫苗獲批上市後,市場還在等待進一步消息。例如第一批商業化疫苗何時上市,是否收費等。
參考國藥集團第一支新冠疫苗於2020年12月30日獲批,並於次日投產第一支中國新冠疫苗。但打破市場預期的是,國内免費接種。
資本市場上漲預期是建立在收費基礎上的,但現在來看,國内全民免費接種,打破市場預期。未來康希諾的「克威莎™」是否免費還有待進一步消息。
另外,還有一部分原因源於今年以來其A股股價已經漲了29.64%,hth登录入口网页股價在短短兩個月内漲幅更是高達106.46%(截至2月26日)。
從另一個角度講可以認為是利好已經在2020年出儘。去年康希諾hth登录入口网页股價漲了近2倍。
就在康希諾還在面臨市場檢驗的時候,同為新冠疫苗概念股的檢測板塊異軍崛起。自2020年以來,板塊最高漲幅萬泰生物漲了近19倍。
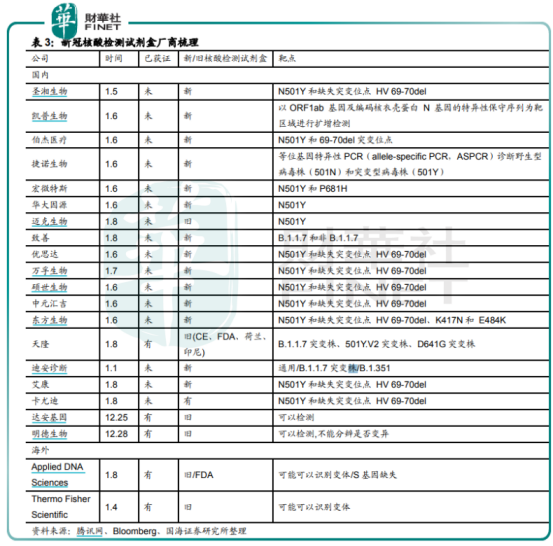
據國海研報數據,2020年3月1日至8月9日我國共出口新冠檢測試劑4.33億人份。
從疫情爆發到2021年1月14日,我國已批準新冠病毒檢測試劑注冊證54個,儀器設備7個,軟 1個;獲得出口白名單的企業472家,其中新冠試劑產品獲歐盟CE認證的482個,獲美國EUA許可的23個,獲澳大利亞TGA認證的3個。
目前我國的核酸檢測試劑日產能為 665.5萬人份以上,抗體檢測試劑日產能為 1546萬人份以上,抗原檢測試劑日產能為190萬人份以上,累計日產能達 2401.5萬人份以上。
國内的核算檢測市場熱度不亞於出口貿易。
2021年年初北方疫情,尤其是石家莊疫情突發之時,華大基因的「火眼實驗室」等檢測起到了有力的篩檢作用。
國内人員流動,需要提供核算檢測報告,為一些第三方檢測機構提供盈利機會。
博市場歡心的是,相較於疫苗免費,這些核酸檢測機構收費介於80-30元之間不等,創造的市場價值不亞於新冠疫苗。
且新冠疫苗還具有高風險、高附加值的特點,藥品的前期研發以及產品從研製、臨床試驗報批到投產的週期長、環節多,容易受到一些不確定性因素的影響。
但也要看到,新冠疫苗免費只是針對接種群眾而言,其實在國家統籌採購下,疫苗費用是由醫保基金和財政共同負擔,主要動用醫保基金滾存結餘。
至於疫苗價格則可以參考2020年12月江蘇省藥品陽光採購價格,彼時在百萬量級採購訂單下,北京科興中維和北京生物製品所均中標,中標價格均為200元。
也就說在批量採購下,疫苗企業還是有利潤可言的。疊加國内新冠疫苗成本低、產能釋放較快,有望複製2020年中國新冠核酸/抗體檢測試劑出口盛況。
財華網所刊載內容之知識產權為財華網及相關權利人專屬所有或持有。未經許可,禁止進行轉載、摘編、複製及建立鏡像等任何使用。
如有意願轉載,請發郵件至content@finet.com.hk,獲得書面確認及授權後,方可轉載。
更多精彩內容,請登陸
財華香港網 (//m.iteamtexas.com/)
財華智庫網(https://www.finet.com.cn)
現代電視 (https://www.fintv.hk)